- Хроматин: Путешествие сквозь стадии развития. Раскрываем секреты ДНК.
- Что такое хроматин и зачем он нужен?
- Роль гистонов в формировании хроматина
- Изменения структуры хроматина в процессе развития
- Роль некодирующих РНК в регуляции хроматина
- Нарушения структуры хроматина и заболевания
- Перспективы терапевтического воздействия на хроматин
Хроматин: Путешествие сквозь стадии развития. Раскрываем секреты ДНК.
Мы часто задумываемся о том, как из одной-единственной клетки получается сложный многоклеточный организм. Как происходит это волшебство дифференцировки, когда клетки, имея одинаковый генетический код, приобретают совершенно разные функции и формы? Ответ кроется в сложном и динамичном мире хроматина – структуры, в которой наша ДНК упакована внутри клеточного ядра. Сегодня мы отправимся в увлекательное путешествие, чтобы исследовать, как хроматин меняется на разных стадиях развития и как эти изменения определяют судьбу каждой клетки.
Представьте себе огромную библиотеку, в которой храняться все знания, необходимые для построения и функционирования живого организма. Эта библиотека – наше ядро клетки, а книги – это гены, составляющие ДНК. Однако, чтобы эта библиотека работала эффективно, необходимо, чтобы книги были правильно организованы и доступны только тем, кому они нужны в данный момент. Хроматин – это как раз та система организации и контроля доступа к генетической информации, которая позволяет клетке правильно развиваться и функционировать.
В этой статье мы рассмотрим, как структура хроматина меняется в процессе развития, как эти изменения влияют на экспрессию генов и как ошибки в регуляции хроматина могут приводить к различным заболеваниям. Приготовьтесь к погружению в мир молекулярной биологии, где мы раскроем секреты одной из самых важных и загадочных структур в наших клетках.
Что такое хроматин и зачем он нужен?
Прежде чем мы углубимся в детали изменений хроматина в процессе развития, давайте разберемся, что же такое хроматин и почему он так важен. Хроматин – это комплекс ДНК, белков (в основном гистонов) и РНК, который находится в ядре эукариотической клетки. Он выполняет несколько ключевых функций:
- Упаковка ДНК: Длина ДНК в одной клетке может достигать нескольких метров, поэтому ее необходимо компактно упаковать, чтобы она поместилась в ядро, размер которого составляет всего несколько микрометров. Хроматин обеспечивает эту компактную упаковку.
- Защита ДНК: Белки хроматина защищают ДНК от повреждений, таких как разрывы и мутации.
- Регуляция экспрессии генов: Хроматин играет ключевую роль в регуляции того, какие гены будут активны в определенный момент времени и в определенной клетке.
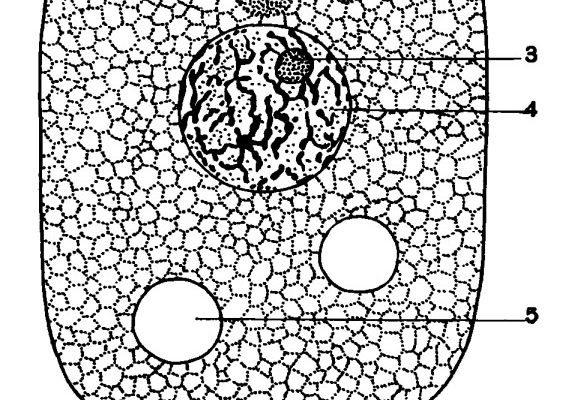
Существует два основных типа хроматина: эухроматин и гетерохроматин. Эухроматин – это более рыхлая форма хроматина, которая содержит активно транскрибируемые гены. Гетерохроматин – это более плотная форма хроматина, которая содержит неактивные гены и повторяющиеся последовательности ДНК.
Соотношение эухроматина и гетерохроматина в клетке может меняться в зависимости от стадии развития и типа клетки. Например, в клетках, которые активно делятся, большая часть хроматина находится в форме эухроматина, чтобы обеспечить доступ к генам, необходимым для репликации ДНК и клеточного деления. В клетках, которые дифференцированы и выполняют определенную функцию, большая часть хроматина может находиться в форме гетерохроматина, чтобы заглушить гены, которые не нужны для выполнения этой функции.
Роль гистонов в формировании хроматина
Гистоны – это основные белки, которые участвуют в формировании хроматина. Существует пять основных типов гистонов: H1, H2A, H2B, H3 и H4. Гистоны H2A, H2B, H3 и H4 образуют октамер, вокруг которого обвивается ДНК, образуя нуклеосому – основную структурную единицу хроматина. Гистон H1 связывается с ДНК между нуклеосомами и способствует дальнейшей конденсации хроматина.
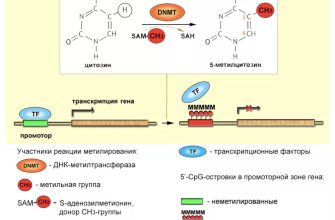
Гистоны могут подвергаться различным химическим модификациям, таким как ацетилирование, метилирование, фосфорилирование и убиквитинирование. Эти модификации могут влиять на структуру и функцию хроматина, а также на экспрессию генов. Например, ацетилирование гистонов обычно связано с активацией генов, а метилирование гистонов может быть связано как с активацией, так и с репрессией генов, в зависимости от того, какой остаток аминокислоты метилирован.
Модификации гистонов – это важный механизм эпигенетической регуляции, который позволяет клеткам изменять экспрессию генов, не изменяя саму последовательность ДНК. Эти эпигенетические изменения могут наследоваться при клеточном делении и играть важную роль в развитии и дифференцировке клеток.
Изменения структуры хроматина в процессе развития
Структура хроматина претерпевает значительные изменения в процессе развития. Эти изменения определяют, какие гены будут активны в определенной клетке и в определенный момент времени, и, таким образом, направляют процесс дифференцировки клеток.
Одним из наиболее важных изменений хроматина в процессе развития является изменение паттернов модификации гистонов. Различные модификации гистонов ассоциированы с различными функциональными состояниями хроматина. Например, ацетилирование гистона H3 на лизине 27 (H3K27ac) обычно связано с активными энхансерами – участками ДНК, которые усиливают экспрессию генов. Метилирование гистона H3 на лизине 27 (H3K27me3) обычно связано с репрессией генов.
В процессе развития клетки приобретают уникальные паттерны модификации гистонов, которые определяют их судьбу. Эти паттерны устанавливаются и поддерживаются различными ферментами, которые добавляют или удаляют модификации гистонов. Например, комплекс Polycomb (PRC2) добавляет метильную группу к гистону H3 на лизине 27 (H3K27me3), что приводит к репрессии генов. Комплекс Trithorax добавляет ацетильную группу к гистону H3 на лизине 27 (H3K27ac), что приводит к активации генов.
Роль некодирующих РНК в регуляции хроматина
Некодирующие РНК (нкРНК) – это молекулы РНК, которые не кодируют белки, но играют важную роль в регуляции экспрессии генов. Некоторые нкРНК, такие как длинные некодирующие РНК (днкРНК), могут взаимодействовать с хроматином и направлять ферменты, модифицирующие гистоны, к определенным участкам генома;
Например, днкРНК Xist играет ключевую роль в инактивации X-хромосомы у самок млекопитающих. Xist связывается с одной из X-хромосом и привлекает комплекс PRC2, который метилирует гистон H3 на лизине 27 (H3K27me3), что приводит к репрессии генов на этой хромосоме.
Другие днкРНК могут участвовать в регуляции экспрессии генов, связанных с развитием и дифференцировкой клеток. Они могут взаимодействовать с различными белками хроматина и влиять на структуру и функцию хроматина в определенных участках генома.
"Эпигенетика – это не судьба, это возможность влиять на свою судьбу."
— Рэнди Джиртл, профессор эпигенетики
Нарушения структуры хроматина и заболевания
Нарушения структуры хроматина могут приводить к различным заболеваниям, включая рак, нейродегенеративные заболевания и нарушения развития. Ошибки в регуляции модификаций гистонов, взаимодействии нкРНК с хроматином или структуре самого хроматина могут привести к неправильной экспрессии генов и нарушению нормального функционирования клеток.
Например, многие виды рака связаны с изменениями в паттернах модификации гистонов. Некоторые виды рака характеризуются гиперметилированием ДНК и гистона H3 на лизине 27 (H3K27me3) в промоторах генов-супрессоров опухолей, что приводит к их репрессии и способствует развитию опухоли. Другие виды рака характеризуются гипометилированием ДНК и гистона H3 на лизине 4 (H3K4me3) в промоторах онкогенов, что приводит к их активации и способствует росту опухоли.
Нарушения структуры хроматина также могут играть роль в развитии нейродегенеративных заболеваний, таких как болезнь Альцгеймера и болезнь Паркинсона. Изменения в модификациях гистонов и структуре хроматина могут влиять на экспрессию генов, связанных с выживанием нейронов и функционированием синапсов, что может приводить к гибели нейронов и развитию нейродегенеративных заболеваний.
Перспективы терапевтического воздействия на хроматин
Понимание роли хроматина в развитии и заболеваниях открывает новые перспективы для разработки терапевтических подходов, направленных на изменение структуры и функции хроматина. Ингибиторы ферментов, модифицирующих гистоны, такие как гистондеацетилазы (HDAC) и гистонметилтрансферазы (HMT), уже используются в клинической практике для лечения некоторых видов рака. Эти препараты могут изменять паттерны модификации гистонов и восстанавливать нормальную экспрессию генов в опухолевых клетках.
Другие перспективные терапевтические подходы включают разработку препаратов, которые могут модулировать взаимодействие нкРНК с хроматином или восстанавливать нормальную структуру хроматина. Эти подходы могут быть использованы для лечения широкого спектра заболеваний, связанных с нарушениями структуры хроматина.
Анализ структуры хроматина при разных стадиях развития – это захватывающая область исследований, которая позволяет нам понять, как из одной-единственной клетки получается сложный многоклеточный организм. Изменения структуры хроматина играют ключевую роль в регуляции экспрессии генов и определяют судьбу каждой клетки. Нарушения структуры хроматина могут приводить к различным заболеваниям, но также открывают новые перспективы для разработки терапевтических подходов, направленных на изменение структуры и функции хроматина.
Мы надеемся, что это путешествие в мир хроматина было для вас познавательным и интересным. Продолжайте исследовать и открывать новые горизонты в науке!
Подробнее
| Хроматин структура | Развитие организма | Гены экспрессия | Гистоны модификации | Эпигенетика регуляция |
|---|---|---|---|---|
| ДНК упаковка | Клеточная дифференцировка | Рак хроматин | Некодирующие РНК | Терапия хроматина |