- Секвенирование in vivo: Путешествие в мир генома через наночастицы
- Что такое секвенирование in vivo?
- Преимущества секвенирования in vivo
- Роль наночастиц в доставке
- Типы наночастиц, используемых для доставки
- Методы секвенирования, используемые in vivo
- Применение секвенирования in vivo
- Диагностика
- Терапия
- Фундаментальные исследования
- Проблемы и перспективы
Секвенирование in vivo: Путешествие в мир генома через наночастицы
Мы живем в эпоху, когда границы науки размываются, и то, что вчера казалось научной фантастикой, сегодня становится реальностью․ Одной из таких прорывных областей является секвенирование in vivo – процесс определения последовательности ДНК непосредственно внутри живого организма․ Это не просто технологический скачок, это потенциальная революция в диагностике, терапии и нашем понимании самой жизни․ Вместо сложных и длительных лабораторных процедур, мы можем заглянуть в генетический код прямо в клетках, где он функционирует․
Но как достичь этой цели? Как проникнуть в микроскопический мир клеток и получить доступ к их генетической информации? Ответ кроется в наночастицах – крошечных, но мощных инструментах, способных доставить необходимые компоненты для секвенирования прямо в нужное место․ Это как отправка микроскопических исследователей вглубь организма, каждый из которых оснащен самым современным оборудованием․
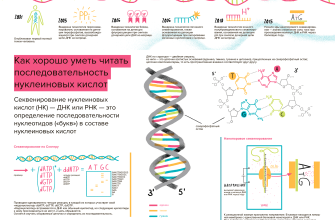
Что такое секвенирование in vivo?
Прежде чем углубиться в детали, давайте определимся с термином․ Традиционное секвенирование требует извлечения ДНК из образца ткани, ее обработки и анализа в лаборатории․ Это может быть трудоемким, дорогостоящим и часто требует значительного времени․ Секвенирование in vivo, напротив, направлено на выполнение этого процесса непосредственно в живых клетках или тканях․
Представьте себе, что вместо того, чтобы отправлять образцы крови в лабораторию, врач может ввести наночастицы, которые считают генетическую информацию в реальном времени и передадут ее на компьютер․ Это открывает двери для мгновенной диагностики, персонализированной медицины и новых способов борьбы с болезнями․
Преимущества секвенирования in vivo
Этот подход имеет ряд значительных преимуществ:
- Минимальная инвазивность: Секвенирование in vivo потенциально менее инвазивно, чем традиционные методы, поскольку требует меньшего количества биологического материала или вообще не требует его․
- Анализ в реальном времени: Позволяет проводить мониторинг генетических изменений в реальном времени, что особенно важно при изучении динамических процессов, таких как развитие рака или реакция на лекарства․
- Сохранение контекста: Сохраняет клеточный контекст, что позволяет изучать ДНК в ее естественной среде и учитывать влияние других молекул и клеточных процессов․
- Персонализированная медицина: Открывает возможности для разработки персонализированных методов лечения на основе генетического профиля конкретного пациента․
Роль наночастиц в доставке
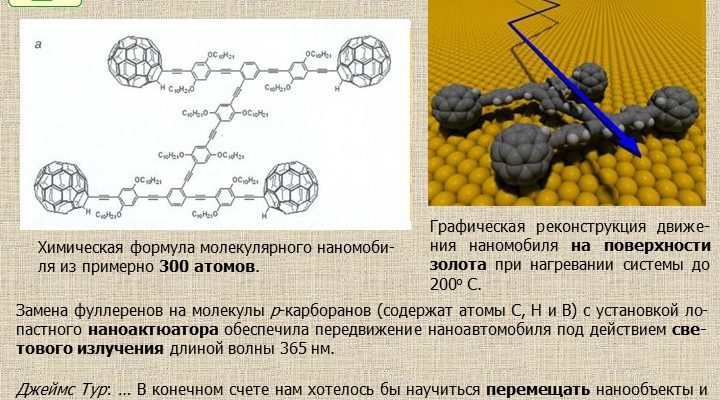
Ключевым элементом секвенирования in vivo является доставка необходимых инструментов и реагентов непосредственно в клетки․ Именно здесь наночастицы играют решающую роль․ Они представляют собой крошечные контейнеры, размером всего несколько нанометров, способные нести различные грузы, включая ферменты, олигонуклеотиды и другие молекулы, необходимые для секвенирования․
Наночастицы могут быть разработаны таким образом, чтобы они специфически нацеливались на определенные типы клеток или тканей․ Это достигается путем модификации поверхности наночастиц лигандами, которые связываются с определенными рецепторами на поверхности клеток․ Представьте себе, что это как отправка почтовой посылки с точным указанием адреса – наночастица доставит свой груз именно туда, где он нужен․
Типы наночастиц, используемых для доставки
Существует множество различных типов наночастиц, которые могут быть использованы для доставки генетического материала in vivo․ Некоторые из наиболее распространенных включают:
- Липосомы: Сферические везикулы, состоящие из липидных бислоев, которые могут заключать водные растворы․
- Полимерные наночастицы: Изготовлены из биоразлагаемых полимеров, которые могут контролируемо высвобождать свой груз․
- Наночастицы золота: Обладают уникальными оптическими свойствами и могут быть использованы для доставки ДНК и других молекул․
- Дендримеры: Высокоразветвленные полимеры с контролируемой структурой, которые могут быть использованы для инкапсуляции и доставки генетического материала․
Выбор конкретного типа наночастиц зависит от множества факторов, включая размер, заряд, стабильность и способность нацеливаться на определенные клетки или ткани․
Методы секвенирования, используемые in vivo
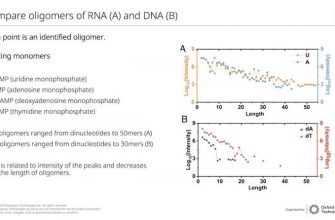
Хотя концепция секвенирования in vivo звучит захватывающе, реализация ее на практике представляет собой серьезную задачу․ Традиционные методы секвенирования, такие как секвенирование по Сэнгеру или секвенирование нового поколения (NGS), требуют предварительной подготовки образцов ДНК в лаборатории․ Однако, разработка методов, которые могут быть применены непосредственно в живых клетках, активно развивается․
Некоторые из наиболее перспективных подходов включают:
- Нанопоровое секвенирование: ДНК пропускается через крошечную пору, и изменение электрического тока, возникающее при этом, используется для определения последовательности нуклеотидов․
- Микроскопия атомно-силовая: Используется для визуализации ДНК на поверхности и определения ее последовательности на основе механических свойств․
- Секвенирование на основе флуоресценции: Молекулы ДНК метятся флуоресцентными красителями, и их последовательность определяется на основе спектра флуоресценции․
Эти методы все еще находятся на стадии разработки, но они демонстрируют большой потенциал для секвенирования in vivo․
"Будущее медицины – это не просто лечение болезней, а предвидение их и предотвращение․" ⸺ Джеймс Уотсон, один из открывателей структуры ДНК
Применение секвенирования in vivo
Потенциальные применения секвенирования in vivo огромны и охватывают широкий спектр областей, от фундаментальных исследований до клинической практики․
Диагностика
Секвенирование in vivo может быть использовано для быстрой и точной диагностики различных заболеваний, включая:
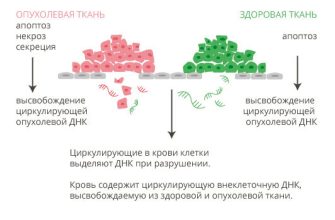
- Рак: Выявление мутаций, связанных с раком, на ранних стадиях развития, мониторинг ответа на терапию и выявление резистентности к лекарствам․
- Инфекционные заболевания: Быстрая идентификация патогенов и определение их генетической устойчивости к антибиотикам․
- Генетические заболевания: Диагностика генетических заболеваний на основе анализа ДНК непосредственно в клетках пациента․
Терапия
Секвенирование in vivo может быть использовано для разработки персонализированных методов лечения, основанных на генетическом профиле конкретного пациента․ Например, оно может быть использовано для:
- Таргетной терапии рака: Разработки лекарств, которые специфически воздействуют на раковые клетки с определенными генетическими мутациями․
- Генной терапии: Доставки генов в клетки для лечения генетических заболеваний․
- Редактирования генома: Использования CRISPR-Cas9 для исправления генетических дефектов непосредственно в клетках․
Фундаментальные исследования
Секвенирование in vivo может быть использовано для изучения фундаментальных биологических процессов, таких как:
- Экспрессия генов: Мониторинг активности генов в реальном времени в различных типах клеток и тканях․
- Взаимодействие ДНК с белками: Изучение взаимодействия ДНК с различными белками, которые регулируют ее функцию․
- Эпигенетические модификации: Анализ эпигенетических изменений ДНК, которые влияют на экспрессию генов․
Проблемы и перспективы
Несмотря на огромный потенциал, секвенирование in vivo сталкивается с рядом серьезных проблем․ Одной из основных проблем является разработка методов секвенирования, которые являются достаточно точными, надежными и чувствительными для применения непосредственно в живых клетках․ Другая проблема заключается в обеспечении эффективной и безопасной доставки наночастиц в нужные клетки или ткани, не вызывая при этом токсических эффектов․
Тем не менее, прогресс в области нанотехнологий, секвенирования и биоинформатики быстро продвигается вперед, и мы можем ожидать значительных достижений в этой области в ближайшие годы․ Секвенирование in vivo может стать мощным инструментом для диагностики, терапии и фундаментальных исследований, открывающим новые горизонты в медицине и биологии․
Мы верим, что будущее за технологиями, которые позволяют нам понимать и взаимодействовать с жизнью на самом глубоком уровне․ Секвенирование in vivo – один из ключевых шагов на этом пути․
Подробнее
| LSI Запрос | LSI Запрос | LSI Запрос | LSI Запрос | LSI Запрос |
|---|---|---|---|---|
| Секвенирование ДНК in vivo | Наночастицы для доставки ДНК | Методы секвенирования in vivo | Применение секвенирования in vivo | Таргетная доставка генов |
| Секвенирование раковых клеток in vivo | Диагностика с использованием наночастиц | Персонализированная медицина и секвенирование | Нанопоровое секвенирование in vivo | Доставка CRISPR in vivo |