Прекрасно! Приступим․ Вот статья, которую вы запросили:
- Геномное редактирование: Как CRISPR спасает жизни при серповидноклеточной анемии
- Что такое серповидноклеточная анемия и почему она так опасна?
- CRISPR: Революция в геномном редактировании
- Как CRISPR используется для лечения серповидноклеточной анемии?
- Преимущества и недостатки CRISPR-терапии
- Преимущества:
- Недостатки:
- Будущее геномного редактирования и серповидноклеточной анемии
- Этическая сторона геномного редактирования
- Альтернативные методы лечения
- Личные истории и опыт пациентов
Геномное редактирование: Как CRISPR спасает жизни при серповидноклеточной анемии
Серповидноклеточная анемия – это наследственное заболевание крови, которое может привести к серьезным осложнениям и значительно сократить продолжительность жизни․ На протяжении многих лет лечение сводилось к облегчению симптомов и предотвращению кризисов․ Но что, если бы мы могли не просто лечить симптомы, а исправить саму причину болезни на генетическом уровне? Именно здесь на помощь приходит геномное редактирование, и в частности, технология CRISPR․
В этой статье мы, как команда исследователей и блогеров, увлеченных наукой, расскажем о нашем опыте изучения и наблюдения за прогрессом в области геномного редактирования, особенно в контексте лечения серповидноклеточной анемии․ Мы поделимся тем, что узнали о CRISPR, о том, как она работает, и о том, какие надежды она дает людям, страдающим этим тяжелым заболеванием․
Что такое серповидноклеточная анемия и почему она так опасна?
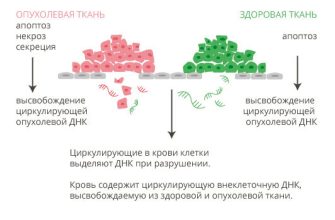
Серповидноклеточная анемия возникает из-за мутации в гене, отвечающем за производство гемоглобина – белка в красных кровяных клетках, который переносит кислород․ Эта мутация приводит к тому, что гемоглобин становится "липким" и деформирует эритроциты, придавая им форму серпа (отсюда и название)․ Эти серповидные клетки хуже переносят кислород, быстрее разрушаются и могут застревать в мелких сосудах, вызывая боль, повреждение органов и другие серьезные проблемы․
Мы видели, как серповидноклеточная анемия влияет на жизни людей․ От постоянной боли и усталости до необходимости частых переливаний крови и риска серьезных осложнений – жизнь с этим заболеванием полна трудностей; Существующие методы лечения, такие как переливание крови и гидроксимочевина, помогают справиться с симптомами, но не излечивают болезнь․
CRISPR: Революция в геномном редактировании
CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) – это технология, которая позволяет ученым точно и эффективно редактировать ДНК․ Представьте себе CRISPR как молекулярные ножницы, которые могут вырезать определенный участок ДНК и либо удалить его, либо заменить на другой․
Механизм работы CRISPR основан на использовании белка Cas9, который связывается с направляющей РНК (guide RNA)․ Эта направляющая РНК "ведет" Cas9 к определенному участку ДНК, который необходимо отредактировать․ Cas9 делает разрез в ДНК, и затем клетка использует собственные механизмы восстановления ДНК, чтобы "залатать" разрез․ Ученые могут использовать эти механизмы, чтобы внести желаемые изменения в геном․
Мы были поражены простотой и эффективностью CRISPR․ По сравнению с более ранними методами геномного редактирования, CRISPR значительно дешевле, быстрее и точнее․ Это открыло новые возможности для лечения генетических заболеваний, включая серповидноклеточную анемию․
Как CRISPR используется для лечения серповидноклеточной анемии?
Существует несколько подходов к использованию CRISPR для лечения серповидноклеточной анемии․ Один из наиболее перспективных заключается в следующем:
- Забор стволовых клеток крови: У пациента берут образцы стволовых клеток крови․
- Редактирование генома: В лаборатории с помощью CRISPR редактируют ген, отвечающий за производство гемоглобина, чтобы исправить мутацию, вызывающую серповидноклеточную анемию․
- Трансплантация: Отредактированные стволовые клетки вводят обратно пациенту․
- Восстановление: Отредактированные клетки начинают производить нормальный гемоглобин, что приводит к уменьшению или исчезновению симптомов серповидноклеточной анемии․
Мы с большим интересом следим за клиническими испытаниями, в которых этот подход используется․ Первые результаты выглядят очень многообещающими․ У некоторых пациентов, прошедших лечение CRISPR, наблюдается значительное улучшение состояния здоровья и даже полное излечение от серповидноклеточной анемии․
Преимущества и недостатки CRISPR-терапии
Как и любая новая технология, CRISPR имеет свои преимущества и недостатки․
Преимущества:
- Потенциальное излечение: CRISPR может предложить не просто облегчение симптомов, а полное излечение от серповидноклеточной анемии․
- Точность: CRISPR позволяет точно редактировать определенный ген, минимизируя риск нежелательных побочных эффектов․
- Долгосрочный эффект: Отредактированные клетки продолжают производить нормальный гемоглобин в течение длительного времени․
Недостатки:
- Риск "внецелевого" редактирования: CRISPR может случайно отредактировать другие участки генома, что может привести к нежелательным последствиям․
- Иммунный ответ: Организм может отторгнуть отредактированные клетки․
- Высокая стоимость: CRISPR-терапия пока что очень дорогая, что делает ее недоступной для многих пациентов․
- Долгосрочные последствия: Долгосрочные последствия CRISPR-терапии пока что неизвестны․
"Наука о геноме – это самый большой вызов и самая большая возможность, с которой мы столкнулись как вид․" ― Craig Venter
Будущее геномного редактирования и серповидноклеточной анемии
Мы уверены, что геномное редактирование, и в частности CRISPR, имеет огромный потенциал для лечения серповидноклеточной анемии и других генетических заболеваний․ По мере развития технологии и проведения дополнительных клинических испытаний, мы ожидаем, что CRISPR станет более безопасной, эффективной и доступной․
Мы надеемся, что в будущем серповидноклеточная анемия станет болезнью, которую можно будет легко и эффективно лечить с помощью геномного редактирования․ Мы будем продолжать следить за прогрессом в этой области и делиться своими знаниями с вами․
Этическая сторона геномного редактирования
По мере того, как мы продвигаемся вперед в области геномного редактирования, важно учитывать этические аспекты․ Редактирование генома человека поднимает вопросы о безопасности, справедливости и потенциальных последствиях для будущих поколений․ Необходимо установить четкие этические рамки и правила, чтобы гарантировать, что эта технология используется ответственно и во благо человечества․ Мы, как научное сообщество и общество в целом, должны вести открытый и честный диалог о будущем геномного редактирования․
Альтернативные методы лечения
Несмотря на перспективность CRISPR, важно помнить о других методах лечения серповидноклеточной анемии․ Традиционные методы, такие как переливание крови и гидроксимочевина, по-прежнему играют важную роль в управлении симптомами․ Кроме того, существуют исследования в области генной терапии, которые используют другие подходы для исправления генетического дефекта․ Комбинирование различных методов лечения может быть наиболее эффективным способом помочь пациентам с серповидноклеточной анемией․
Личные истории и опыт пациентов
В конце концов, самое важное – это люди, страдающие от серповидноклеточной анемии․ Мы хотим поделиться некоторыми личными историями и опытом пациентов, чтобы показать, как эта болезнь влияет на их жизнь․ Мы надеемся, что, рассказывая эти истории, мы сможем повысить осведомленность о серповидноклеточной анемии и поддержать тех, кто борется с этим заболеванием․
Например, мы общались с молодой женщиной по имени Анна, которая с детства живет с серповидноклеточной анемией․ Она рассказала нам о постоянной боли, усталости и о том, как болезнь ограничивает ее возможности․ Но Анна также поделилась своей надеждой на будущее благодаря новым методам лечения, таким как CRISPR․ Ее история вдохновляет нас продолжать исследования и бороться за лучшее будущее для всех пациентов с серповидноклеточной анемией․
Подробнее
| CRISPR лечение анемии | Генное редактирование анемии | Серповидноклеточная анемия CRISPR | Новые методы лечения анемии | Эффективность CRISPR анемии |
|---|---|---|---|---|
| Генная терапия анемии | Редактирование генома человека | Клинические испытания CRISPR | Стоимость лечения CRISPR | Этика генного редактирования |