- Секвенирование In Vivo: Наночастицы как Ключ к Генетическому Будущему?
- Что такое Секвенирование In Vivo?
- Наночастицы: Ключевые Игроки в Секвенировании In Vivo
- Типы Наночастиц, Используемых в Секвенировании In Vivo
- Методы Секвенирования In Vivo с Использованием Наночастиц
- Преимущества и Недостатки Секвенирования In Vivo
- Преимущества:
- Недостатки:
- Перспективы и Будущее Секвенирования In Vivo
Секвенирование In Vivo: Наночастицы как Ключ к Генетическому Будущему?
Приветствую вас, друзья! Сегодня мы погрузимся в захватывающий мир, где нанотехнологии встречаются с генетикой, открывая невиданные ранее перспективы. Речь пойдет о секвенировании in vivo – революционном подходе, который может изменить наше понимание о геноме и его функционировании. Мы, как любопытные исследователи, всегда ищем новые горизонты, и эта тема, безусловно, одна из самых интересных, что мы встречали за последнее время.
Представьте себе возможность читать генетический код непосредственно внутри живого организма, без необходимости извлекать клетки и проводить сложные лабораторные процедуры. Это звучит как научная фантастика, но благодаря развитию наночастиц, это становится реальностью. Мы разберем, что такое секвенирование in vivo, как работают наночастицы в этой области, и какие перспективы и вызовы стоят перед этой технологией.
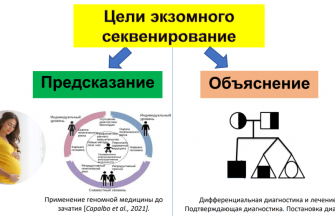
Что такое Секвенирование In Vivo?
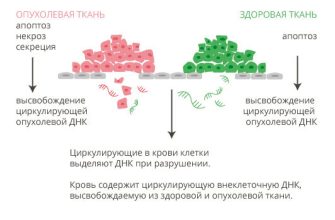
Традиционное секвенирование ДНК требует извлечения генетического материала из организма, его подготовки и анализа в лаборатории. Этот процесс может быть долгим, трудоемким и, что самое важное, может не отражать реальную картину генетических процессов, происходящих в живом организме в реальном времени. Секвенирование in vivo, напротив, стремится обойти эти ограничения.
Суть секвенирования in vivo заключается в использовании наночастиц для доставки сенсоров или реагентов непосредственно в клетки или ткани живого организма. Эти сенсоры могут взаимодействовать с ДНК или РНК, позволяя в реальном времени отслеживать генетические изменения, активность генов или мутации. Представьте себе, что мы можем "подслушать" генетический разговор клеток, не вмешиваясь в их естественную среду. Это открывает беспрецедентные возможности для понимания биологических процессов.
Наночастицы: Ключевые Игроки в Секвенировании In Vivo
Наночастицы – это структуры размером от 1 до 100 нанометров. Их малый размер и уникальные физико-химические свойства делают их идеальными кандидатами для доставки грузов внутрь клеток. В контексте секвенирования in vivo, наночастицы выполняют несколько важных функций:
- Доставка: Наночастицы могут быть спроектированы так, чтобы целенаправленно доставлять сенсоры или реагенты к определенным клеткам или тканям. Это особенно важно при изучении конкретных органов или опухолей.
- Защита: Наночастицы могут защищать чувствительные молекулы от деградации ферментами или иммунной системой организма. Это увеличивает эффективность секвенирования и снижает вероятность побочных эффектов.
- Визуализация: Некоторые наночастицы могут быть визуализированы с помощью различных методов, таких как флуоресценция или магнитно-резонансная томография (МРТ). Это позволяет отслеживать их перемещение в организме и контролировать процесс секвенирования.
- Взаимодействие: Наночастицы могут быть функционализированы для специфического взаимодействия с ДНК или РНК. Например, они могут содержать олигонуклеотиды, комплементарные определенным последовательностям генов.
Типы Наночастиц, Используемых в Секвенировании In Vivo
Существует множество различных типов наночастиц, которые могут быть использованы в секвенировании in vivo. Выбор конкретного типа зависит от задачи исследования, типа клеток или тканей, которые необходимо исследовать, и доступных методов визуализации. Вот некоторые из наиболее распространенных типов:
- Липосомы: Сферические везикулы, состоящие из липидных бислоев. Они хорошо переносятся организмом и могут быть использованы для доставки широкого спектра молекул.
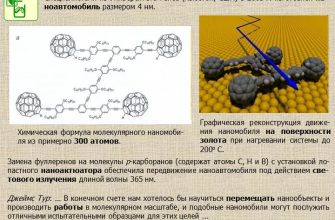
- Наночастицы золота: Инертные и нетоксичные наночастицы, которые могут быть легко функционализированы и визуализированы. Они обладают уникальными оптическими свойствами, которые делают их полезными для флуоресцентной микроскопии.
- Квантовые точки: Полупроводниковые нанокристаллы, которые обладают высокой яркостью и фотостабильностью. Они могут быть использованы для многоцветной визуализации и отслеживания нескольких целей одновременно.
- Магнитные наночастицы: Наночастицы, содержащие магнитные материалы, такие как оксид железа. Они могут быть использованы для доставки лекарств или генов под действием магнитного поля, а также для МРТ.
- Дендримеры: Разветвленные полимеры с контролируемой структурой. Они могут быть использованы для доставки больших молекул, таких как ДНК и РНК.
Методы Секвенирования In Vivo с Использованием Наночастиц
Не существует единого "золотого стандарта" для секвенирования in vivo. Различные исследовательские группы разрабатывают свои собственные методы, основанные на различных типах наночастиц, сенсоров и методов визуализации. Однако, большинство методов включают следующие этапы:
- Синтез и функционализация наночастиц: Наночастицы синтезируются и функционализируются с помощью молекул, которые обеспечивают адресную доставку к определенным клеткам или тканям, а также взаимодействие с ДНК или РНК.
- Визуализация и отслеживание: Перемещение наночастиц в организме отслеживается с помощью различных методов визуализации, таких как флуоресцентная микроскопия, МРТ или позитронно-эмиссионная томография (ПЭТ).
- Сбор данных: Сенсоры, доставленные наночастицами, собирают данные о генетической активности или мутациях. Эти данные могут быть переданы на внешнее устройство или обработаны непосредственно внутри организма.
- Анализ данных: Собранные данные анализируются для получения информации о генетическом статусе клеток или тканей.
"Будущее принадлежит тем, кто верит в красоту своей мечты." — Элеонора Рузвельт
Преимущества и Недостатки Секвенирования In Vivo
Как и любая новая технология, секвенирование in vivo имеет свои преимущества и недостатки. Рассмотрим их подробнее:
Преимущества:
- Анализ в реальном времени: Секвенирование in vivo позволяет отслеживать генетические процессы в реальном времени, что невозможно при традиционных методах секвенирования.
- Сохранение естественной среды: Этот метод не требует извлечения клеток из организма, что позволяет сохранить их естественную среду и избежать артефактов, связанных с культивированием клеток in vitro.
- Адресная доставка: Наночастицы могут быть спроектированы для адресной доставки сенсоров к определенным клеткам или тканям, что позволяет изучать генетические процессы в конкретных областях организма.
- Ранняя диагностика: Секвенирование in vivo может быть использовано для ранней диагностики заболеваний, таких как рак, путем обнаружения мутаций на ранних стадиях.
- Персонализированная медицина: Эта технология может быть использована для разработки персонализированных методов лечения, основанных на генетическом профиле конкретного пациента.
Недостатки:
- Токсичность наночастиц: Некоторые наночастицы могут быть токсичными для организма, что ограничивает их применение. Необходимы дальнейшие исследования для разработки безопасных и биосовместимых наночастиц.
- Иммунный ответ: Организм может реагировать на наночастицы как на инородные тела, вызывая иммунный ответ. Необходимо разрабатывать методы для уменьшения иммуногенности наночастиц.
- Сложность разработки: Разработка эффективных наночастиц и сенсоров для секвенирования in vivo является сложной и дорогостоящей задачей.
- Ограниченная глубина проникновения: Некоторые методы визуализации, используемые в секвенировании in vivo, имеют ограниченную глубину проникновения в ткани, что ограничивает их применение для изучения глубоко расположенных органов.
- Этическая дилемма: Использование секвенирования in vivo вызывает этические вопросы, связанные с конфиденциальностью генетической информации и возможностью манипулирования геномом.
Перспективы и Будущее Секвенирования In Vivo
Несмотря на существующие вызовы, секвенирование in vivo обладает огромным потенциалом и может произвести революцию в различных областях, от фундаментальной биологии до клинической медицины. Мы видим, что эта технология движется вперед семимильными шагами, и вот некоторые из перспективных направлений:
- Разработка новых наночастиц: Исследования направлены на разработку новых, более безопасных и биосовместимых наночастиц с улучшенными характеристиками доставки и визуализации.
- Разработка новых сенсоров: Разрабатываются новые сенсоры, способные обнаруживать широкий спектр генетических изменений и взаимодействовать с ДНК и РНК с высокой специфичностью.
- Комбинирование с другими технологиями: Секвенирование in vivo может быть комбинировано с другими технологиями, такими как оптогенетика и хемогенетика, для контроля генетической активности и изучения поведения клеток.
- Применение в клинической медицине: Секвенирование in vivo может быть использовано для ранней диагностики и мониторинга заболеваний, разработки персонализированных методов лечения и оценки эффективности терапии.
- Изучение старения: Эта технология может быть использована для изучения генетических изменений, происходящих в процессе старения, и разработки методов для замедления старения и продления жизни.
Мы верим, что секвенирование in vivo – это не просто научная фантастика, а реальная технология, которая в ближайшем будущем станет неотъемлемой частью нашей жизни. Она откроет новые возможности для понимания генетических процессов, разработки новых методов лечения и улучшения качества жизни.
Подробнее
| LSI Запрос 1 | LSI Запрос 2 | LSI Запрос 3 | LSI Запрос 4 | LSI Запрос 5 |
|---|---|---|---|---|
| Наночастицы для доставки ДНК | Секвенирование in vivo раковых клеток | Методы визуализации наночастиц in vivo | Токсичность наночастиц in vivo | Применение секвенирования in vivo |
| Доставка генов in vivo | Наночастицы в генетической терапии | In vivo секвенирование РНК | Новые методы секвенирования in vivo | Наночастицы для адресной доставки |